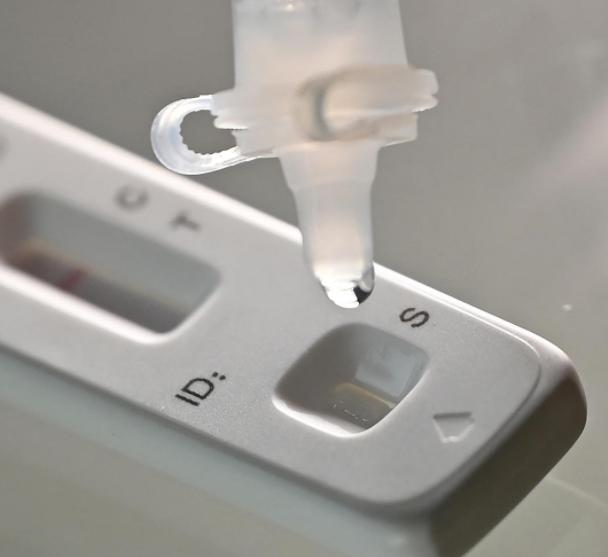
Op 12 Maartth 2022, dieNMPA (SFDA) het 'n kennisgewing uitgereik wat die verandering van aansoek vir selftoetsing van COVID-19-antigeenprodukte deur Nanjing Vazyme Biotech goedkeurCo., Bpk, Beijing Jinwofu Bioingenieurswese TegnologieCo., Bpk, Shenzhen Huada Yinyuan Farmaseutiese Tegnologie Co., Ltd, Guangzhou Wondfo Biotech Co., Ltd enBeijing Savant Biotechnology Co., Ltd(Huaketai).Vyf COVID-19-antigeen-selftoetsprodukte is bekendgestel.
Op 11 Maart 2022 het die NHC aangekondig dat die Omvattende Span van die Gesamentlike voorkoming en beheermeganisme van die Staatsraad besluit het om die nuwe Coronavirus-toetsstrategie verder te optimaliseer en die behoeftes van COVID-19-voorkoming en -beheer te dien. antigeentoetsing tot nukleïensuurtoetsing en het "die toepassingsprotokol vir nuwe koronavirus-antigeenopsporing (proef)" gemaak
Die protokol spesifiseer die toepaslike populasie vir antigeentoetsing:
Eerstens, diegene wat primêre mediese instellings besoek en simptome soos asemhalingskanaal en koors het binne 5 dae na die aanvang van simptome;
Tweedens, kwarantynwaarnemingspersoneel, insluitend tuiskwarantynwaarneming, noue kontak en sub-nou kontak, toegangskwarantynwaarneming, inperkingsgebied en beheerareapersoneel;
Die derde is die gemeenskapsinwoners wat die behoefte het vir antigeen-selfopsporing.
Wenke:Antigeenopsporing is 'n belangrike aanvulling van nukleïensuuropsporing, maar die resultate van antigeenselfopsporing kan nie as basis vir die diagnose van infeksie gebruik word nie
Postyd: 22 Maart 2022